Nucleic Acids Research | 陈庭坚/梅辉团队合作开发非天然核酸(XNA)固相酶促合成平台
近日,中国科学院深圳先进技术研究院合成生物学研究所梅辉副研究员团队联合华南理工大学生物科学与工程学院陈庭坚教授团队在酶促非天然核酸(XNA)的高效合成技术开发上取得新突破,相关成果发表在国际顶级期刊Nucleic Acids Research杂志(IF=16.7)上,题目为“A Solid-Phase Enzymatic Synthesis Platform for the Facile Production of 2'-Fluoroarabinonucleic Acid (FANA) and Chimeric XNA Oligonucleotides Using an Evolved XNA Polymerase”。中国科学院深圳先进技术研究院合成生物学研究所梅辉副研究员和华南理工大学生物科学与工程学院陈庭坚教授为共同通讯作者,华南理工大学博士生张彬良和副研究员杜宇辉为论文的共同第一作者。

文章上线截图
论文链接:https://doi.org/10.1093/nar/gkaf567
非天然核酸(XNA),如2'-氟代阿拉伯核酸(FANA),凭借其独特的稳定性与功能性,在生物医药、合成生物学及纳米技术等领域展现出广阔的应用前景。然而,其广泛应用受限于现有合成方法的瓶颈。传统的固相化学合成法存在效率低、成本高、环境污染大等问题。近年来,包括陈庭坚教授团队在内的多个研究团队已经对不同家族的DNA聚合酶和RNA聚合酶进行了分子改造,获得了能够识别并加工多种非天然底物的XNA聚合酶突变株,并基于此开发了一系列非天然寡核苷酸的酶法制备策略。然而,现有的酶法合成技术则常面临DNA引物和模板去除困难、产物纯度不佳等挑战。因此,开发高效、绿色的XNA合成技术是领域内亟待解决的难题。
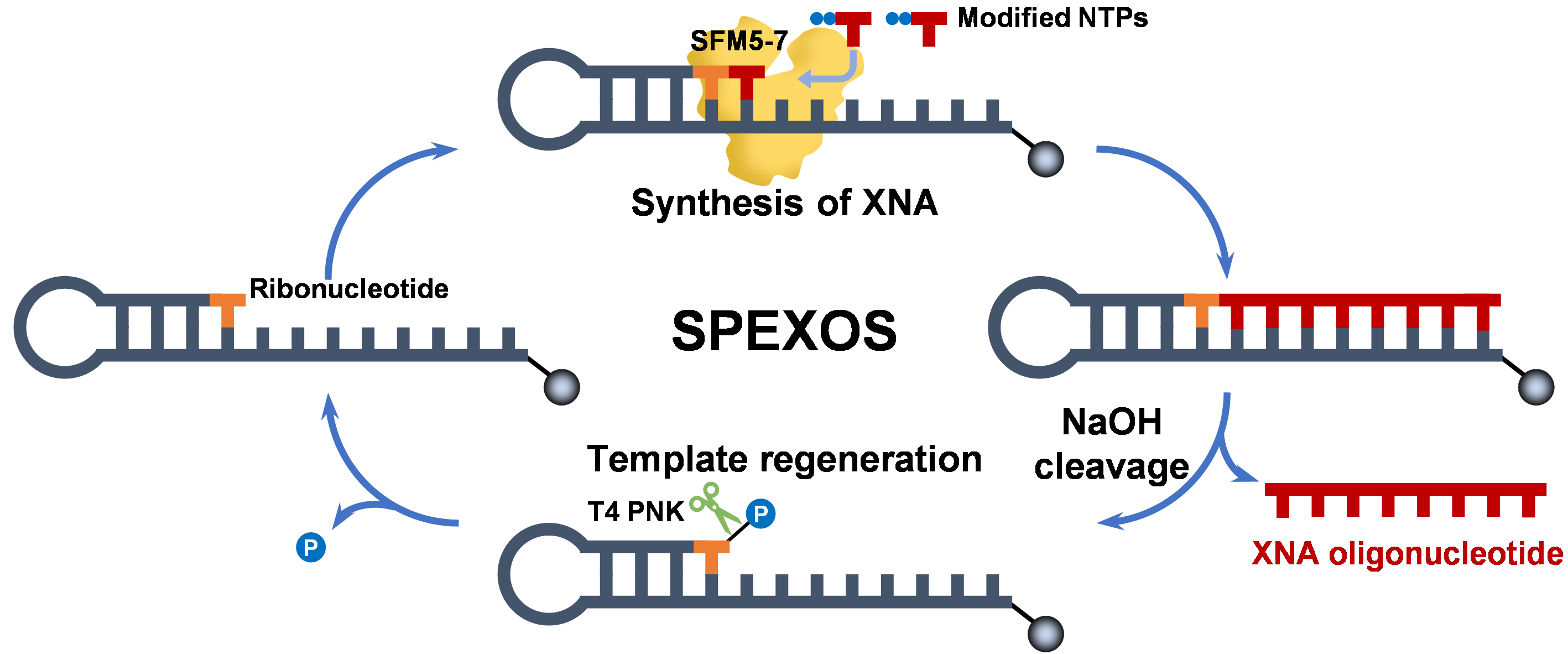
图1. 基于高效非天然核酸聚合酶的固相酶促XNA寡核苷酸合成(SPEXOS)平台
在本工作中,团队首先系统评估了四种实验室进化的SF变体(SFM4-3、SFM4-6、SFM4-9和SFM5-7)以DNA为模板合成不同长度FANA的催化活性。通过稳态动力学实验和测序分析,进一步表征了活性最优突变株SFM5-7合成FANA的催化效率与保真度,证实其具备卓越的合成性能。上述结果及团队前期研究结果表明,SFM5-7能够高效、高保真地催化包括FANA在内的多种XNA的合成。基于此,课题组创新性地开发了固相酶促XNA寡核苷酸合成(SPEXOS)平台。该平台的核心思路是结合核糖核苷酸插入与碱性裂解步骤:首先利用SFM5-7在自合成引发发夹DNA模板的3'端精确引入一个核糖核苷酸;随后将该模板固定于磁珠上,利用SFM5-7在固相表面高效合成目标XNA链(如FANA、2'-F-RNA、2'-OMe-RNA等);最后,利用氢氧化钠特异性裂解核糖核苷酸3'端的磷酸二酯键,温和释放高纯度的XNA产物。值得一提的是,通过T4多聚核苷酸激酶(T4 PNK)处理去除模板末端的磷酸基团,可实现模板的再生与循环利用(经2-4轮循环,产物收率仍可达初始轮的69-88%),显著提高了XNA合成的可持续性和经济性。
随后,团队对该平台的普适性进行了进一步验证。该平台不仅成功高效合成了纯合的FANA、2'-F-RNA、2'-OMe-RNA,更实现了2'-F-RNA/2'-OMe-RNA、FANA/DNA、FANA/2'-F-RNA、FANA/2'-F-RNA/2'-OMe-RNA、FANA/DNA/2'-OMe-RNA和FANA/DNA/2'-F-RNA/2'-OMe-RNA等多种复杂嵌合XNA的可控合成,这些产物大多难以通过依赖DNA酶的传统策略获得。此外,利用该平台,团队还实现了5'端单标记(如EdU或dCAm标记)和双标记(EdU和dCAm标记)的FANA的高效酶法制备,并在此基础上实现了FANA的各种5'端功能化,为功能化XNA的开发与应用提供了新工具。接着,团队还利用该平台成功制备出了具有催化活性的FANA核酶(FANAzyme),充分证实了该平台生产功能性XNA分子的能力。
该研究开发的SPEXOS平台为XNA的绿色、高效、可持续生产及5′末端标记和功能化提供了新策略。它有效解决了现有技术的关键瓶颈,避免了昂贵有毒试剂的使用,无需复杂的模板设计,产物纯度高,操作简便,且模板可循环利用。该平台能够灵活合成纯合XNA、嵌合XNA及其标记产物,为非天然核酸(XNA)在生物医药(如高效制备siXNA和XNA适配体药物),分子诊断(如开发高稳定性XNA探针和生物传感器),合成生物学(如开发各类XNA功能元件)和生物材料(如高效制备各类XNA纳米结构器件)等领域的全面应用提供了必需的工具和技术平台。
该工作得到了广东省“珠江人才计划”引进创新创业团队、广东省“珠江人才计划”青年拔尖人才项目、国家自然科学基金、国家重点研发计划、广州市科技计划项目、广东省合成基因组学重点实验室、深圳合成基因组学重点实验室、深圳合成生物学创新研究院等项目的资助。
